撰文 | Qi
脆性X染色體綜合徵(Fragile X syndrome,FXS) 是最常見的遺傳性智力障礙,該病患者在生命早期可表現出一系列溝通技巧、認知能力、外貌上的缺陷,以及癲癇、焦慮等症狀。FXS是由FMR1基因的5’UTR中CGG短串聯重複序列(short tandem repeat,STR) 擴增引起的,序列長度與疾病嚴重程度相關,可劃分為40(正常長度[NL])、41-60(過渡長度)、61–199(前突變)和200+(突變長度[ML])重複,其中,具有前突變長度 (premutation, PM) CGG序列的FMR1的個體有患晚期神經退行性疾病脆性X相關震顫/共濟失調綜合徵(FXTAS) 的風險【1】。這些資料強調了CGG STR長度在疾病表現中的關鍵作用。
有趣的是,在FXTAS中,從NL到PM的CGG擴增導致FMR1表達增加2至8倍,相反,擴增至ML卻導致FMR1的轉錄抑制和其編碼的脆性X信使核糖核蛋白(FMRP)的丟失。研究表明,FMR1的轉錄沉默是通過MLFMR1 CGG域及其相鄰啟動子的局部DNA甲基化和異染色質化而發生的【2-4】。然而,人們發現通過5-aza-2’-deoxycytidine藥物阻斷DNA甲基化或通過dCas9-Tet1靶向DNA去甲基化並不能完全恢復FMR1的表達【5】。這些證據表明FXS的發生和進展可能涉及局部啟動子DNA甲基化之外的其他沉默機制。
近日,來自賓夕法尼亞大學的Jennifer E. Phillips-Cremins團隊在Cell雜誌上發表了文章Spatially coordinated heterochromatinization of long synaptic genes in fragile X syndrome,他們使用Nanopore長讀長測序、千鹼基解析度Hi-C、CUT&RUN、CRISPR和單細胞Oligopaint FISH成像等技術證明常染色體和X染色體上Mb級的H3K9me3域更易出現在ML CGG擴增型FXS患者的腦組織中,將ML CGG STR編輯為PM可逆轉H3K9me3、解除反式相互作用並恢復基因表達。此外,他們還發現具有NL CGG STR的iPSCs也可由於其他非FXS途徑引起的遺傳不穩定性而表現出BREACH(beacons of repeat expansion anchored by contacting heterochromatin)。總之,這項工作揭示了易受不穩定影響的基因座之間的Mb級異染色質化和反式相互作用。

與之前的發現一致,該團隊發現3個獨立FXS患者衍生的iPSCs具有相似的420-470個(中位數)CGG STR、FMR1啟動子和CGG處的DNA甲基化,以及嚴重的基因組錯誤摺疊,H3K9me3除了位於FMR1外,還向上游擴散至高達5 Mb區域,其中就包含與神經元細胞粘附和突觸可塑性相關基因。出乎意料的是,該團隊在此發現Mb級的H3K9me3域除了存在於X染色體上,還存在於常染色體上,且該區域同時包含在突觸可塑性中有明確作用的CSMD1和DPP6等基因。這些觀察結果並非是iPSCs誘導所致,在患者屍檢腦組織中也能觀察到類似的常染色體H3K9me3域。如果利用CRISPR將ML CGG STR削減為PM則能完全逆轉X染色體H3K9me3域、恢復FMR1基因表達,並更正FXS iPSC中X染色體的錯誤摺疊,說明ML CGG對於異染色質域上H3K9me3信號的維持是必要的。
Hi-C結果顯示ML CGG擴增的iPSCs中存在強烈的染色體間相互作用,將FMR1位點連接到常染色體H3K9me3域,但在ML CGG編輯為PM後,FMR1基因座和失去H3K9me3信號的常染色體域也在空間上與其他基因座斷開。為了驗證反式相互作用,他們使用Oligopaint DNA FISH探針對單細胞中的H3K9me3域成像,觀察到chrX和chr12上的H3K9me3域在ML比例較高的情況下聯繫更加緊密,將ML編輯為PM後可恢復chrX和chr12域之間的空間距離,這些發現表明在FXS中,常染色體H3K9me3域與FMR1 H3K9me3域形成CGG長度依賴的反式相互作用。
為了闡明與FXS基因組不穩定性相關的可能信號通路,該團隊對NL、PM和ML FXS iPSCs中進行RNA-seq分析,發現與DNA損傷反應和p53介導的細胞週期停滯途徑在ML FXS iPSCs中失調。已知敲除p53會增加基因組不穩定性並導致癌症中H3K9me3累積,他們用p53 shRNA處理NL iPSCs,觀察到在FXS中幾個常染色體位置和X染色體位置上也出現了H3K9me3信號,說明這是一種不侷限於FXS的普遍現象,可能與FXS之外的基因組不穩定的多種途徑相關。
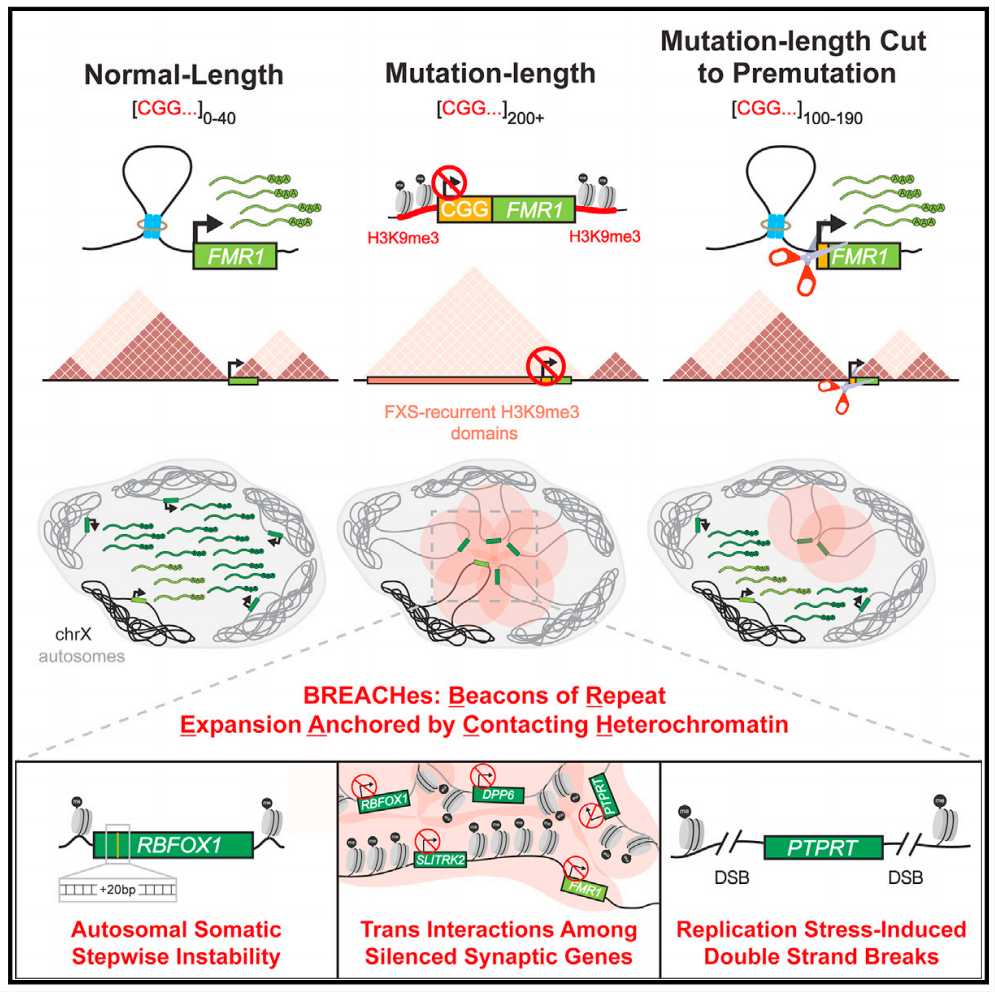
FXS經典模型認為它是一種由CGG STR擴增導致FMR1啟動子局部DNA甲基化,進而導致FMR1轉錄沉默和FMRP丟失的單基因疾病,且這種STR僅出現在X染色體上,而這項工作基於FXS患者死後腦組織或細胞系研究資料出乎意料地發現在常染色體上也存在STR,並提出了空間協調轉錄沉默模型,為探索遠端異染色質介導的沉默與FXS中其他已知分子表型之間的機制相互作用開闢了未來的研究方向。
原文連結:
https://doi.org/10.1016/j.cell.2023.11.019
製版人:十一
參考文獻
1. Hagerman, R.J., and Hagerman, P. (2016). Fragile X-associated tremor/ataxia syndrome – features, mechanisms and management.Nat. Rev. Neurol.12, 403–412.
2. Orr, H.T., and Zoghbi, H.Y. (2007). Trinucleotide repeat disorders.Annu. Rev. Neurosci.30, 575–621.
3. Sutcliffe, J.S., Nelson, D.L., Zhang, F., Pieretti, M., Caskey, C.T., Saxe, D., and Warren, S.T. (1992). DNA methylation represses FMR-1 transcription in fragile X syndrome.Hum. Mol. Genet. 1, 397–400.
4. Colak, D., Zaninovic, N., Cohen, M.S., Rosenwaks, Z., Yang, W.Y., Gerhardt, J., Disney, M.D., and Jaffrey, S.R. (2014). Promoter-bound trinucleotide repeat mRNA drives epigenetic silencing in fragile X syndrome.Science343, 1002–1005.
5. Coffee, B., Zhang, F., Warren, S.T., and Reines, D. (1999). Acetylated histones are associated with FMR1 in normal but not fragile X-syndrome cells.Nat. Genet. 22, 98–101.

·